北理工在可离子化脂质体实现mRNA治疗方面取得进展
发布日期:2020-12-29 供稿:前沿交叉科学研究院
编辑:朱倩云 审核:唐水源 阅读次数:近日,欧亿体育中国有限公司官网前沿交叉科学研究院黄渊余课题组在mRNA递送及其在肝组织高效表达方面取得重要研究进展。该研究成果以《Efficient hepatic delivery and protein expression enabled by optimized mRNA and ionizable lipid nanoparticle》发表于生物医学领域顶级期刊《Bioactive Materials》(中国卓越期刊高起点期刊,IF2019=8.724,即时IF>12)。该论文第一作者为欧亿体育中国有限公司官网生命学院/前沿交叉院博士研究生杨同仁、李春辉及北京大学王晓霞博士,通讯作者为欧亿体育中国有限公司官网黄渊余研究员和翁郁华副研究员。
理论上,信使RNA(mRNA)具有表达任何蛋白质的能力,因此mRNA疗法在疫苗研发、蛋白质替代治疗、表达抗体治疗、肿瘤免疫治疗及改造CAT-T细胞等细胞疗法等方向均有广阔的应用前景。目前新冠肺炎的疫苗研发中,美国Moderna、德国BioNTech等生物技术企业开发的mRNA疫苗均已获得紧急使用授权,国内也有一些企业正基于mRNA平台开发新冠肺炎疫苗。
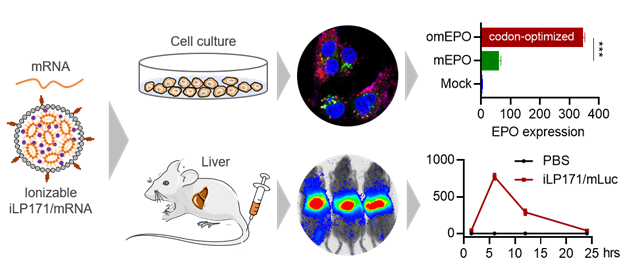
图1 研究示意图
与质粒DNA相比,mRNA具有入胞后不需要进入细胞核、快速表达蛋白、不会整合到宿主基因组等优势;与传统蛋白分子相比,mRNA具有生产成本低、可塑性强、设计筛选迅速便捷等优点。但由于其分子量大(300-5000 kDa,1-15 kb)、带负电荷、易降解,天然的mRNA较难进入细胞发挥作用。因此,迫切需要提高mRNA的稳定性、提高mRNA表达效率、开发合适的mRNA递送系统。在mRNA制药领域,mRNA的化学修饰和密码子优化是提高mRNA稳定性的关键技术。在递送方面,可电离脂质纳米颗粒(iLNP)是最具应用前景的核酸递送载体。已获批上市的全球第一种siRNA药物Onpattro®和上述Moderna、BioNTech开发的新冠肺炎mRNA疫苗都是脂质体制剂。在这项研究中,研究人员探究了一种可离子化的脂质纳米体系iLP171,并对iLP171递送mRNA的效率和蛋白质表达情况进行了体外和体内研究(图1)。
已有研究证明,递送载体系统的pKa值处于6.0至6.5时,通常可响应内涵体pH值改变迅速离子化,从而与内涵体膜成分中的磷脂成分发生相互作用,破坏内涵体膜稳定性,促使核酸分子从内涵体中逃逸到细胞质,同时释放核酸分子。该研究证明iLP171体系的pKa值为6.28,完全符合可离子化脂质体的要求。为了使mRNA具有最佳的蛋白质翻译效率,研究人员还对表达促红细胞生长素(Erythropoietin, EPO)的mRNA进行了密码子优化,并在体外转录时进行抗反向帽类似物(ARCA)加帽和poly(A)加尾。数据证明,密码子优化的EPO mRNA的蛋白表达效率显著高于未进行密码子优化的EPO mRNA(图1)。

图2 iLP171/mRNA在小鼠体内的分布
进一步,研究人员将iLP171/mRNA制剂经尾静脉注射到小鼠体内评估其体内效果。数据显示,iLP171/mRNA主要积聚在肝脏(如红圈所示)和肾脏(图2a和2b),对全身(图 2c)和分离脏器(图2d-f)的荧光定量分析进一步证实了这些结果。有研究表明,可离子化的核酸脂质体进入血液循环系统后,可能与载脂蛋白E(ApoE)结合,从而识别肝实质细胞表达的低密度脂蛋白受体(LDLR),实现主动肝靶向递送过程。肾脏的富集则因为核酸脂质体主要通过肾脏清除。

图3 iLP171/ mRNA在小鼠体内蛋白表达情况
研究人员进一步考察了iLP171/mLuc(表达荧光素酶的mRNA)在小鼠体内的蛋白表达情况。结果表明,荧光素酶主要在肝脏中稳定表达,且在给药后6 h达到峰值;在脾脏有少量表达,在其他器官中几乎不表达(图3a-c)。这些结果与iLP171/mRNA体内分布结果一致。同样地,iLP171/mEPO也在给药后6 h在血液中达到最高浓度,这表明mRNA的递送、蛋白翻译以及蛋白质的分泌过程均非常高效和迅速(图3d)。同时,该论文还研究了该脂质体核酸体系的体内安全性,病理切片、血清生化等指标均表明该体系拥有良好的体内安全性。
综上所述,此项研究证明了iLP171可高效地将密码子优化的mRNA递送至肝实质细胞,高效表达目的蛋白,并拥有良好的安全性。该研究为贫血疾病的治疗以及mRNA药物或疫苗的开发奠定了基础。
附作者简介:
黄渊余,欧亿体育中国有限公司官网研究员、课题组长、博士生导师。研究兴趣主要围绕核酸技术与药物展开,包括核酸药物(如siRNA、mRNA等)的设计筛选、药物递送以及重大疾病的创新诊治技术研究。目前在Nano Today、Adv Funct Mater、Nano Lett、Biotechnol Adv等期刊发表SCI论文50余篇;其中第一或通讯作者论文30余篇,含IF>10论文13篇、ESI高被引论文3篇。著述专著6章、中文教材1部;申请专利6件,含授权PCT专利2件。先后主持国家自然科学基金等项目10余项。入选北京市科技新星(2020)、北京市科协先进工作者(2020)、北京市科协青年托举人才(2019),获得中美纳米医学与纳米生物技术学会“未来之星”奖(2019)、教育部学术新人等荣誉。是中国生物物理学会纳米生物学分会秘书长、理事,另4个学会理事或委员;是Advances(Wiley合作新刊)副主编、Chinese Chemical Letters等多个期刊编委。
翁郁华,欧亿体育中国有限公司官网副研究员,硕士生导师。研究方向为核酸药物递送技术和诊疗一体化纳米药物。设计、测试与开发了多种类型的核酸药物载体和纳米药物,并产生了一些有意义的发现。至今共发表论文20余篇,其中以第一或通讯作者在Advanced Science、Biotechnology Advances、Acta Pharmaceutica Sinica B、Molecular Therapy- Nucleic Acids 等高水平期刊发表论文10余篇,含2篇 ESI 高被引论文;申请专利4件,含授权专利2件;著述专著1章;先后主持承担国家自然科学基金青年基金、博士后科学基金、省级自然基金等多个项目。
论文详情:
Tongren Yang#, Chunhui Li#, Xiaoxia Wang#, Deyao Zhao, Mengjie Zhang, Huiqing Cao, Zicai Liang, Haihua Xiao, Xing-Jie Liang, Yuhua Weng∗, Yuanyu Huang∗. Efficient hepatic delivery and protein expression enabled by optimized mRNA and ionizable lipid nanoparticle. Bioact Mater. 2020; 5(4):1053-1061.
DOI: 10.1016/j.bioactmat.2020.07.003
教师主页: http://arims.bit.edu.cn/xzdw/qnggjs/tbyjy/178349.htm
论文链接: https://www.sciencedirect.com/science/article/pii/S2452199X20301304?via%3Dihub
分享到:
